Paparan Topik | Vaksinasi Covid-19
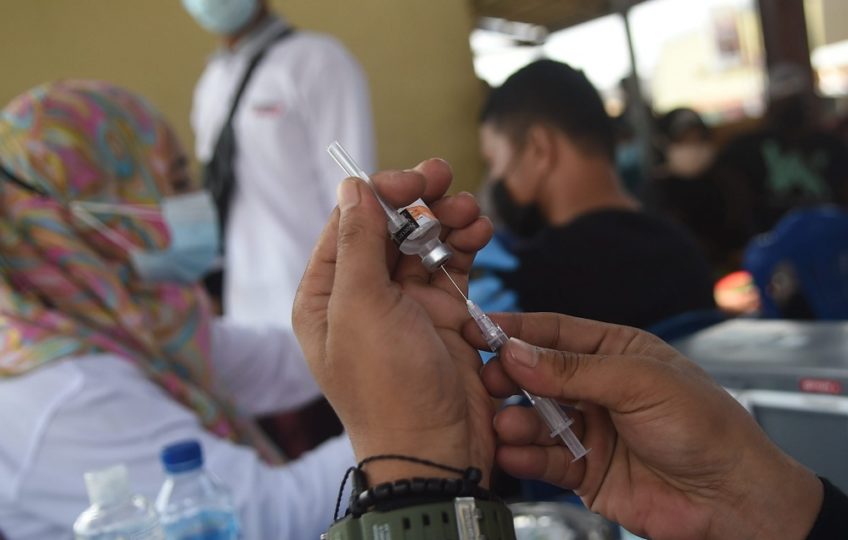
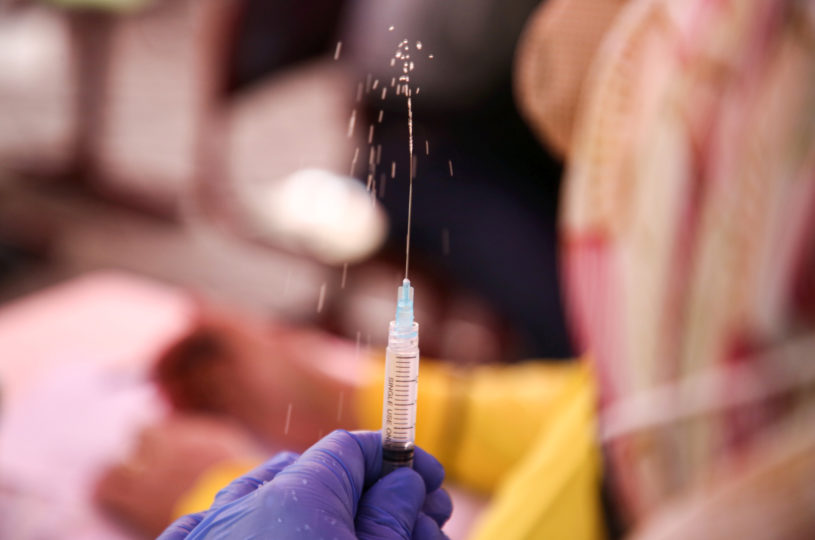
Vaksin AstraZeneca untuk Covid-19: Kronologi Kasus Pembekuan Darah Pascavaksinasi dan Perkembangan Penggunaannya di Indonesia
Penggunaan vaksin AstraZeneca untuk Covid-19 sempat ditunda di berbagai negara di Eropa karena adanya laporan pembekuan darah pascavaksinasi. Namun, manfaat vaksin tersebut dianggap lebih besar daripada risiko yang ada sehingga direkomendasikan untuk terus digunakan, termasuk di Indonesia. Vaksin AstraZeneca telah masuk daftar vaksin yang dapat digunakan dalam kondisi darurat oleh World Health Organization atau WHO.